
“Ho gettato via la mia tazza quando ho visto un bambino che beveva al ruscello dalle proprie mani.”
— Socrate
Il presente articolo si propone di esplorare le nuove terapie sviluppate per i bambini nati pretermine, concentrandosi su un modello animale rivoluzionario utilizzato per lo studio dei deficit neurologici correlati a questa condizione. Attraverso la ricerca condotta dall’Istituto Italiano di Tecnologia, sono emersi risultati promettenti che potrebbero aprire nuove prospettive nel trattamento di tali disturbi. In particolare, verrà esaminata la scoperta di un farmaco potenzialmente utile e l’importanza di sviluppare una ‘placenta artificiale‘ per mitigare gli effetti negativi della prematurità. Infine, sarà presentato il ganaxolone come nuovo approccio terapeutico per affrontare i deficit cognitivi e comportamentali associati ai bambini nati pretermine.
L’introduzione del modello animale per lo studio dei deficit neurologici dei prematuri
L’introduzione del modello animale per lo studio dei deficit neurologici dei prematuri rappresenta un’importante svolta nella ricerca scientifica. Grazie a questo approccio, gli scienziati sono riusciti a studiare in modo più accurato e dettagliato i disturbi neurologici che possono colpire i bambini nati pretermine. Utilizzando animali appositamente selezionati come modelli, è stato possibile replicare le condizioni di sviluppo tipiche della prematurità e analizzare gli effetti sul sistema nervoso centrale. Questo metodo ha permesso di identificare le alterazioni neurali e le conseguenti disfunzioni cognitive e comportamentali che spesso si manifestano nei bambini prematuri. Grazie a questi studi, si è potuta acquisire una maggiore comprensione delle cause dei deficit neurologici legati alla prematurità e si sono aperte nuove prospettive per lo sviluppo di terapie mirate ed efficaci.
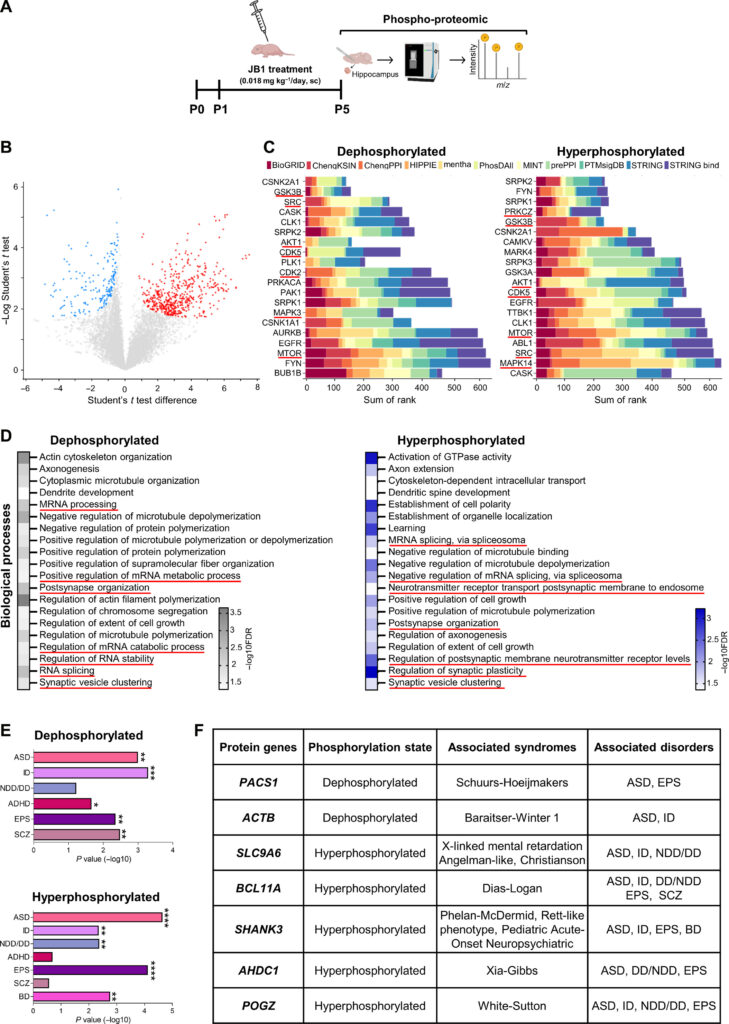
Potenzieri, A., Uccella, S., Preiti, D., Pisoni, M., Rosati, S., Lavarello, C., … Cancedda, L. (n.d.). Early IGF-1 receptor inhibition in mice mimics preterm human brain disorders and reveals a therapeutic target. Science Advances, 10(9), eadk8123. doi:10.1126/sciadv.adk8123
I risultati promettenti dello studio condotto dall’Istituto Italiano di Tecnologia
Lo studio condotto dall’Istituto Italiano di Tecnologia ha riportato risultati promettenti nel campo delle terapie per i bambini nati pretermine. Gli scienziati hanno utilizzato un modello animale per studiare i deficit neurologici che colpiscono i prematuri, e hanno osservato miglioramenti significativi dopo il trattamento con il ganaxolone, un nuovo farmaco. I risultati mostrano che il ganaxolone è in grado di ridurre i deficit cognitivi e comportamentali tipici dei bambini nati pretermine. Questo rappresenta un passo avanti importante nella ricerca di nuove terapie per migliorare la qualità di vita di questi bambini. Tuttavia, ulteriori studi sono necessari per confermare l’efficacia del farmaco e valutarne gli eventuali effetti collaterali. Nonostante ciò, i risultati ottenuti fino ad ora offrono una speranza concreta per il futuro dei bambini nati pretermine e delle loro famiglie.
La scoperta di un farmaco potenzialmente utile come trattamento
La scoperta di un farmaco potenzialmente utile come trattamento rappresenta una svolta significativa nel campo delle terapie per i bambini nati pretermine. Lo studio condotto dall’Istituto Italiano di Tecnologia ha identificato un composto chiamato ganaxolone, che sembra essere in grado di migliorare i deficit cognitivi e comportamentali tipici dei prematuri. Il ganaxolone agisce sul sistema nervoso centrale, modulando i recettori del GABA, un neurotrasmettitore coinvolto nella regolazione dell’attività cerebrale. I risultati preliminari dello studio sono promettenti, dimostrando che l’uso del ganaxolone nei modelli animali ha portato a miglioramenti significativi nelle capacità cognitive e comportamentali. Tuttavia, ulteriori ricerche sono necessarie per valutare l’efficacia e la sicurezza di questo farmaco negli esseri umani. La scoperta del ganaxolone apre la strada a nuove possibilità terapeutiche per i bambini nati pretermine, offrendo la speranza di un miglioramento delle loro condizioni neurologiche.
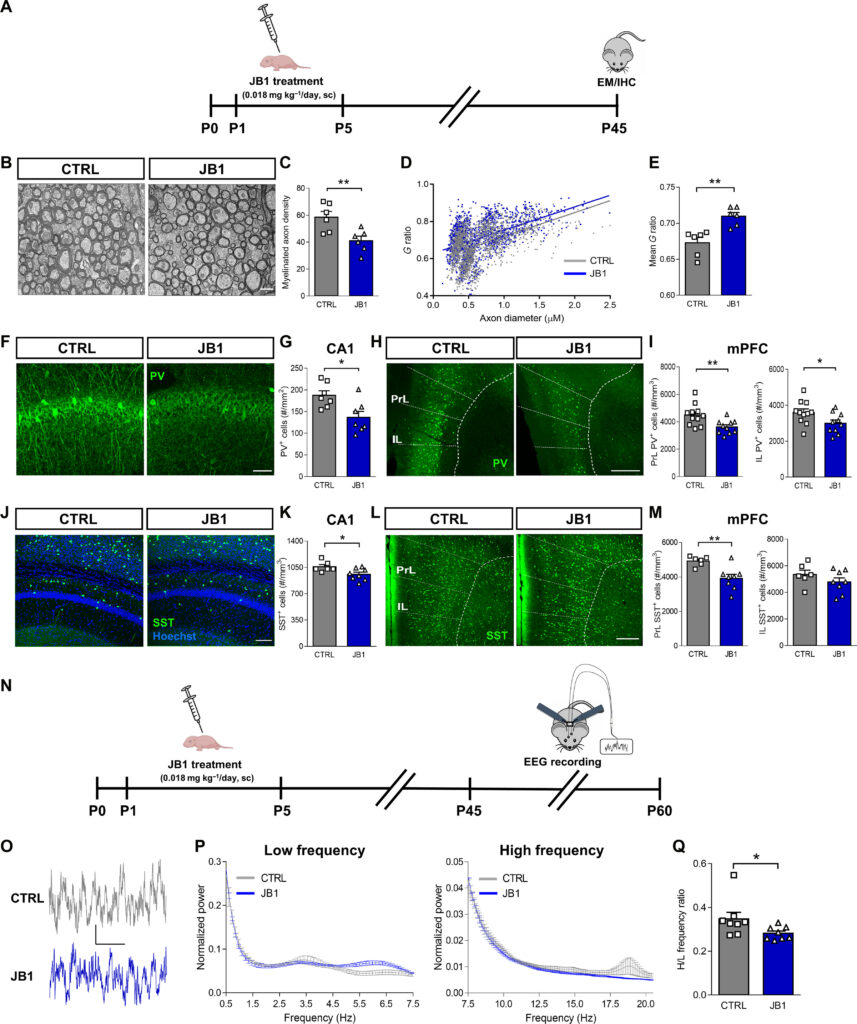
La necessità di una ‘placenta artificiale’ per ridurre gli effetti negativi della prematurità
La prematurità rappresenta una condizione che può causare gravi conseguenze neurologiche e cognitive nei bambini nati prima del termine. Per affrontare questa sfida, gli scienziati hanno cercato di sviluppare nuovi approcci terapeutici, tra cui l’utilizzo di una ‘placenta artificiale‘. Questo dispositivo, che simula l’ambiente uterino, potrebbe fornire un ambiente ottimale per lo sviluppo del feto prematuro, riducendo così gli effetti negativi della prematurità. La placenta artificiale potrebbe essere in grado di fornire il sostegno necessario per il corretto sviluppo dei polmoni e del sistema nervoso centrale, consentendo ai bambini prematuri di completare la loro crescita in modo più simile a quanto avverrebbe nel grembo materno. Questa innovativa tecnologia potrebbe rappresentare un importante passo avanti nella cura dei bambini nati pretermine e offrire loro maggiori possibilità di sviluppo sano e senza complicazioni.
Il ganaxolone: un nuovo approccio terapeutico per i deficit cognitivi e comportamentali
Il ganaxolone rappresenta un nuovo approccio terapeutico promettente per il trattamento dei deficit cognitivi e comportamentali nei bambini nati pretermine. Questo farmaco, ha dimostrato risultati positivi in uno studio condotto su un modello animale. Il ganaxolone agisce sul sistema GABA, un neurotrasmettitore coinvolto nel controllo dell’eccitabilità neuronale. Grazie alle sue proprietà anticonvulsivanti e ansiolitiche, questo composto potrebbe essere in grado di migliorare le funzioni cognitive e comportamentali compromesse nei bambini nati pretermine. Tuttavia, ulteriori ricerche sono necessarie per valutare la sua efficacia e sicurezza nell’uso clinico. Se i risultati saranno confermati negli studi futuri, il ganaxolone potrebbe rappresentare una nuova opportunità terapeutica per migliorare la qualità di vita di questi bambini e delle loro famiglie.
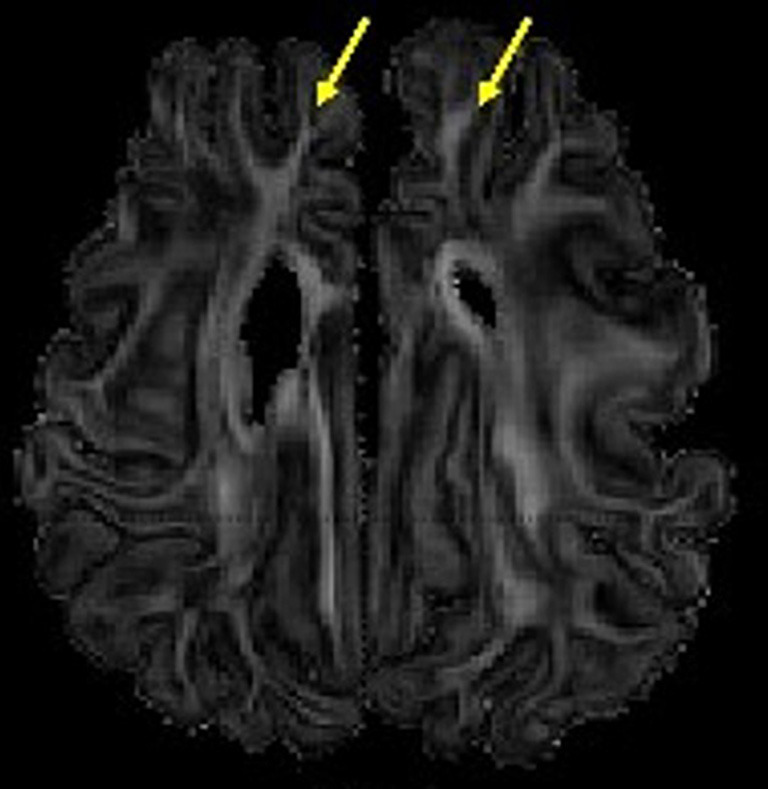
Fallon BP, Mychaliska GB. Development of an artificial placenta for support of premature infants: narrative review of the history, recent milestones, and future innovation. Transl Pediatr. 2021 May;10(5):1470-1485. doi: 10.21037/tp-20-136. PMID: 34189106; PMCID: PMC8192990.
In conclusione…
In un panorama scientifico sempre in evoluzione, la ricerca sulle terapie per i bambini nati pretermine rappresenta una luce di speranza. Grazie all’introduzione di un modello animale rivoluzionario, gli scienziati sono riusciti a ottenere risultati promettenti nello studio dei deficit neurologici dei prematuri. In particolare, la scoperta del ganaxolone come potenziale trattamento apre nuove prospettive per affrontare i deficit cognitivi e comportamentali che possono affliggere questi bambini. Tuttavia, rimane ancora molto da fare. La necessità di una ‘placenta artificiale‘ per ridurre gli effetti negativi della prematurità è un argomento che merita ulteriori approfondimenti e ricerche. Inoltre, è importante considerare l’impatto sociale ed economico di queste nuove terapie e assicurarsi che siano accessibili a tutti i bambini nati pretermine. Sono necessari sforzi congiunti da parte della comunità scientifica, dei governi e delle organizzazioni sanitarie per garantire che ogni bambino abbia la possibilità di svilupparsi al meglio delle sue potenzialità.





